生物由来製品感染等被害救済制度の概要
医薬品、医療機器及び再生医療等製品は、今日医療上必要不可欠なものとして国民の生命、健康の保持増進に大きく貢献しています。そのうち、ヒトや動物等、生物に由来するものを原料や材料とした医薬品や医療機器である生物由来製品、並びに再生医療等製品(生物由来製品等)については、ウイルス等の感染の原因となるものが入り込むおそれがあることから、様々な安全性を確保するための措置が講じられてきております。しかしながら、最新の科学的な知見に基づいて安全対策が講じられたとしても、生物由来製品等による感染被害を完全になくすことはできません。
このような背景から、2004年4月1日に生物由来製品感染等被害救済制度が創設されました。2004年4月1日以降(再生医療等製品については2014年11月25日以降)に生物由来製品等を適正に使用したにもかかわらず発生した感染等により、入院治療が必要な程度の疾病や日常生活が著しく制限される程度の障害等の健康被害を受けた方の救済を図ることを目的として医療費、医療手当、障害年金等の救済給付を行う公的な制度です。
手続きの流れ
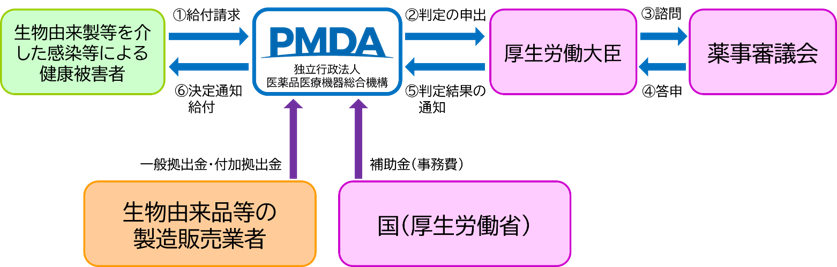
給付の請求
健康被害を受けた本人(または遺族)等が、請求書、その他請求に必要な書類(診断書等)をPMDAに送付することにより、医療費等の給付の請求を行います。給付の種類に応じて、請求の期限や請求に必要な書類等が定められています。
医学・薬学的な判定
PMDAは、給付の請求があった健康被害について、その健康被害が生物由来製品等を介した感染等によるものかどうか、生物由来製品等が適正に使用されたかどうか等の医学・薬学的な判定の申し出を厚生労働大臣に行い、厚生労働大臣はPMDAからの判定の申し出に応じ、薬事審議会(副作用・感染等被害判定部会)に意見を聴いて判定することとされています。
迅速な救済を図るため、厚生労働大臣への判定の申し出にあたって、PMDAは、請求内容の事実関係の調査・整理(請求内容の事実関係調査、症例経過概要表の作成、調査報告書の作成等)を行っています。
給付の決定
PMDAは、厚生労働大臣による医学・薬学的判定に基づいて給付の支給の可否を決定します。なお、この決定に対して不服がある者は、支給の決定があったことを知った日の翌日から起算して三月以内に厚生労働大臣に対して審査を申し立てることができます。
拠出金
医療費等の給付に必要な費用は、許可生物由来製品製造販売業者及び感染拠出金に係る許可再生医療等製品製造販売業者からの拠出金で賄われています
なお、生物由来製品感染等被害救済制度に係るPMDAの事務費の二分の一相当額については、国からの補助金により賄っています。
