医薬品や医療機器などの安全と安心の向上
医薬品や医療機器などは、私たちが健やかで幸せな生活を送るうえで必要不可欠なものです。
科学技術の進歩により私たち人類はさまざまな困難を乗り越えてきました。医薬品や医療機器などは、いわば人類の叡智の結晶であり、これらを通じてさまざまな疾病を克服してきたと言えます。
しかしながら、医薬品や医療機器などは、基本的に私たちの身体に何らかの影響を及ぼして病気の治療や診断などを行うものであり、それが期待どおりの治療効果などとして現れる一方で、期待しない影響として副作用などが起こることは避けられません。
医薬品や医療機器などは、医療上のリスクとベネフィットのバランスの上で使用されるものであり、医療関係者には医薬品や医療機器などの適正な使用が常に求められます。医薬品や医療機器などの「安全」は、医薬品や医療機器などに携わる人々の日々のたゆまぬ努力を通じて築かれていくものであり、それが使用者の「安心」につながるものと考えます。
PMDAは、厚生労働省と連携して、医薬品や医療機器などの「安全」と「安心」の向上に全力で貢献します。
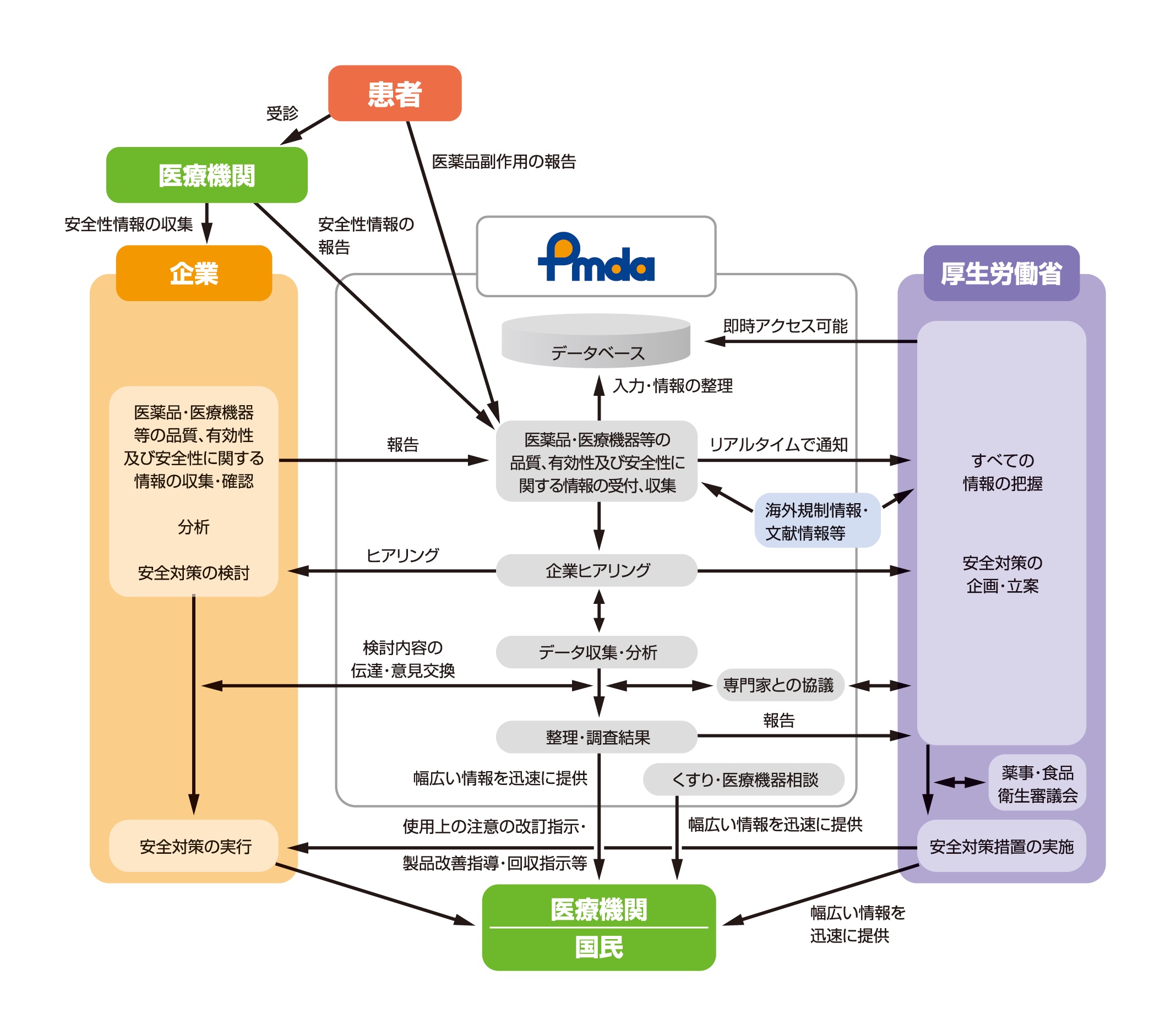
安全性情報の一元的収集:情報収集・整理業務
医薬品や医療機器などの安全性情報の収集にあたっては、広い範囲から、必要な情報を、必要なタイミングで収集することが重要です。
当機構は、市販後の医薬品や医療機器などによる副作用・不具合・感染症や、開発段階で発生した副作用などに関する企業からの報告について、IT技術を活用してこれらを電子的に受け付けるなど、一連の安全性情報を迅速かつ効率よく収集します。
また、医療機関からの安全性情報、日米EU医薬品規制調和国際会議(ICH)などにおける国際的情報、医学・薬学に関する学会報告、研究報告など、必要な安全性情報を幅広く、一元的に収集します。収集した情報は、速やかにデータベース化するなど整理し、厚生労働省と共有します。
科学的な調査と検討:調査・検討業務
安全性情報の調査や検討にあたっては、収集した情報をいかに科学的に評価するかが重要です。そのために当機構は、疫学的手法による解析など最新の科学的評価手法を導入し、さらに研修などを通じて職員の専門性を高め、安全対策業務の質の維持・向上につとめます。
収集した情報について、高い専門性を有する職員による科学的分析を通じ、緊急に対応が必要な案件はないか、医療上のリスクとベネフィットのバランスは保たれているか、最善の安全対策として何をすべきかなど、企業へのヒアリングや必要に応じた専門家への意見聴取などを通じ、当機構は、医薬品や医療機器などの安全対策に資する調査・検討を行います。
また、審査等部門や救済部門と必要な連携を図り、さらには厚生労働省とも連携して、的確な安全対策を行います。
的確なアドバイス:相談業務
医薬品や医療機器などを安全かつ安心して使用するためには、企業における情報収集・検討・措置が日頃から確実に実施できる体制、危機管理体制の確立が必要不可欠です。
PMDAは、個別の医薬品や医療機器などの添付文書の改訂や、重篤な副作用発生を防ぐための適正使用の推進、医療安全など、医薬品や医療機器などの安全性向上に関する企業からの相談を幅広く受け、企業に対し的確な助言・指導を行い、個別の医薬品や医療機器などの安全性向上を図るとともに、企業の安全対策に関する体制の向上に貢献します。
また、国民の皆様から、医薬品や医療機器について安全性などの相談に応じ、適切なアドバイス、適切な情報提供につとめます。
必要な情報をタイムリーに:情報提供業務
医薬品や医療機器などを安全かつ安心して使用するためには、必要な情報が、必要な方にタイムリーに提供される必要があります。
PMDAは、当ホームページにおいて、医療用医薬品や医療機器の添付文書情報を網羅的に掲載するとともに、その改訂がなされたときには早急にその情報を掲載します。
また、医薬品や医療機器の回収情報、厚生労働省が発表した緊急安全性情報、報道発表資料、新薬の承認に関する情報、医療用医薬品の品質に関する情報、医療安全に資する情報など、医薬品や医療機器などの品質、有効性、安全性などに関する情報を、広く、積極的に提供するようつとめます。