医療機器とは

医療機器製造販売と医療機器クラス分類の関係は?
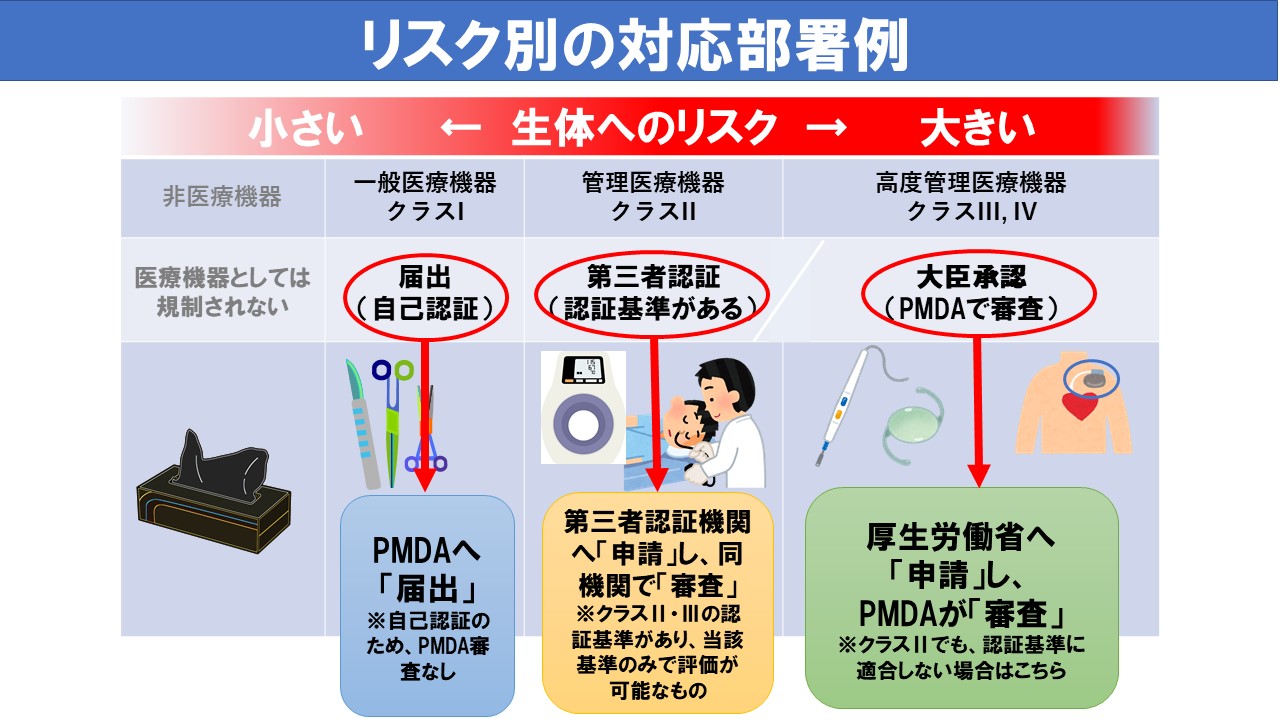
医療機器の製造販売にあたっては、患者へのリスクの高さに応じて、手続きが異なっています。
- 一般医療機器(クラスI)とは、不具合が生じた場合でも、人体へのリスクが極めて低いと考えられるもので、PMDAへの届出を行うことで製造販売が可能です。
- 管理医療機器(クラスII)とは、不具合が生じた場合でも、人体へのリスクが比較的低いと考えられるもので、それらのうち、認証基準のあるものの製造販売にあたっては、第三者認証機関による認証が必要です。
- 高度管理医療機器(クラスIII)とは、不具合が生じた場合、人体へのリスクが比較的高いと考えられるもの及び高度管理医療機器(クラスIV)不具合が生じた場合、患者への侵襲性が高く、生命の危険に直結する恐れがあるものの製造販売にあたっては、厚生労働大臣の承認が必要であり、それらについてPMDAが審査を行っています。
なお、2014年11月25日より、クラスIIIの高度管理医療機器のうち、認証基準のあるものについては、第三者認証機関による認証が可能となりました。
医療機器ユニットでは、医療機器を開発、製造販売を目指す方々に向け、講習会や説明会を定期的に開催しております。
詳しくは、こちらをご覧ください。
審査について
審査ポイント
医療機器関連通知について
医療機器の製造販売手続きについて
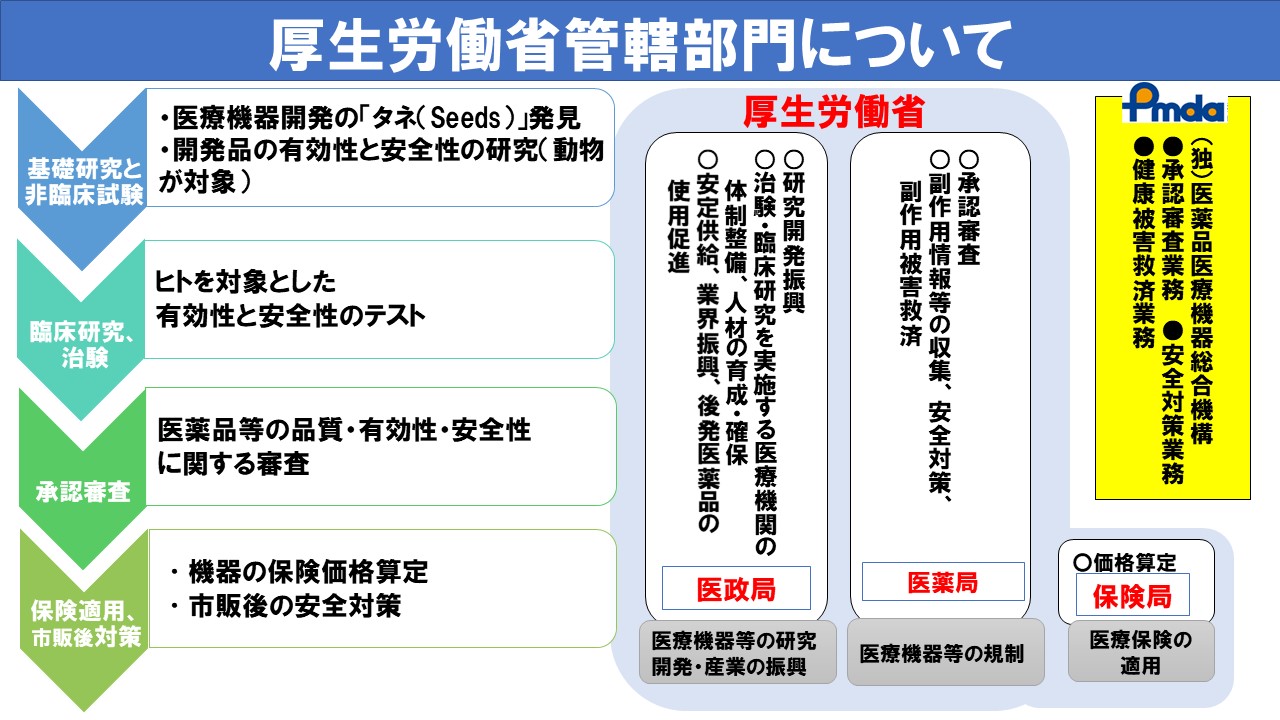
PMDAと厚生労働省の連携について
よくある質問


<上記URLリンク先>
その他、講習会・説明会資料はこちらを参考にしてください。
