2024年5月1日
独立行政法人 医薬品医療機器総合機構
1. 調査対象の範囲
公財)日本医療機能評価機構(以下、「評価機構」という。)による医療事故情報収集等事業報告書中の記述情報及び評価機構ホームページ上の公開データ中の医療機器に関連する医療事故及びヒヤリ・ハット事例
1)医療事故関係について
評価機構による医療事故情報収集等事業第73回及び第74回報告書(以下、「当該報告書」という。)中の記述情報並びに評価機構ホームページ上の公開データから抽出した2023年1月1日から6月30日の間に報告された事例。
2)ヒヤリ・ハット事例関係について
当該報告書に掲載された2023年1月1日から6月30日の間に報告された事例。
3)その他
当該報告書に掲載された医療機器にかかる以下の事例。
- ダブルチェックに関連した事例
- 手術中に皮膚保護剤を塗布後、術野で電気メスを使用した際に引火した事例
- 輸液ポンプ使用中、ルートを延長した後にクレンメの開放を忘れ、薬剤が投与されなかった事例
- 抗がん剤投与中にMRI検査を実施する際、ケモセーフロックに金属探知機が反応した事例
- 小児の輸液の血管外漏出
- 酸素残量の確認不足
- CVポート留置術の際、術野の消毒をしていなかった事例
- ミキシング中にシリンジのガスケットを破損し、ルート内に空気が混入した事例
- MRI検査時の高周波電流のループによる熱傷
2. 検討方法
医療機器に起因するヒヤリ・ハット等の事例について、医療機器としての観点から安全対策に関する専門的な検討を行うため、各医療関係職能団体代表、学識経験者等の専門家及び製造販売業者の代表から構成される標記検討会を開催し、医療機器の物的要因に対する安全管理対策について検討した。
3. 調査結果
- 医療機器毎の事例数について
調査対象の各事例において使用されている医療機器毎に、各事例の報告者意見に基づく事故の内容及び事故の程度を分類し、まとめた結果を図1から図4、表1及び表2に示す。
また、表1及び表2においては、各医療機器におけるヒューマンエラー・ヒューマンファクターに起因する事例の事故の程度と内容の内訳を示している。
なお、参考として過去に報告されたドレーン・チューブ及びドレーン・チューブ以外の医療機器の年度別累積件数を参考1から参考2に示す。
図1 ドレーン・チューブにおける事故の内容の内訳
|
集計対象期間:2022年7月1日から12月31日 |
集計対象期間:2023年1月1から6月30日 |
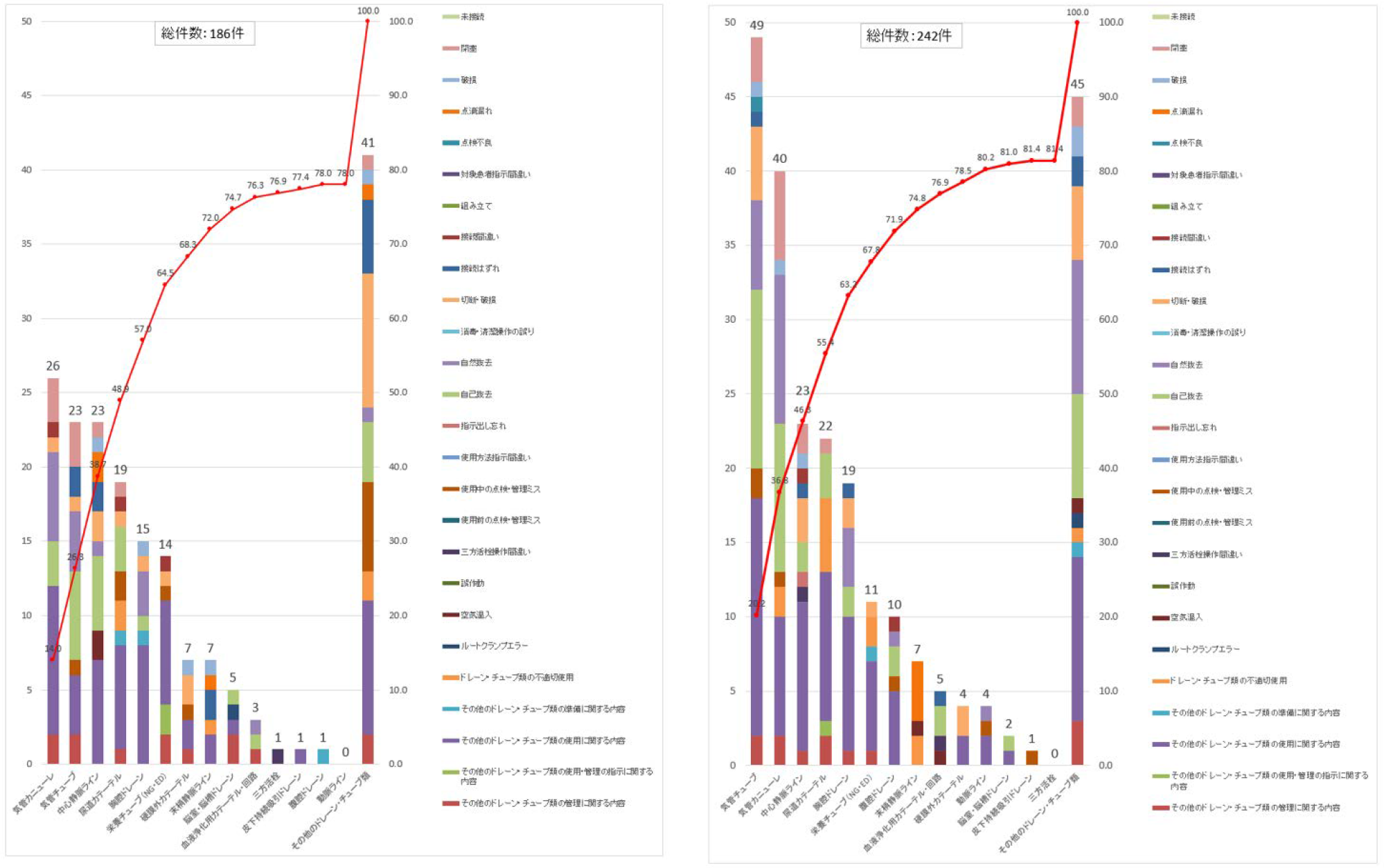
図2 ドレーン・チューブにおける事故の程度の内訳
|
集計対象期間:2022年7月1日から12月31日 |
集計対象期間:2023年1月1日から6月30日 |
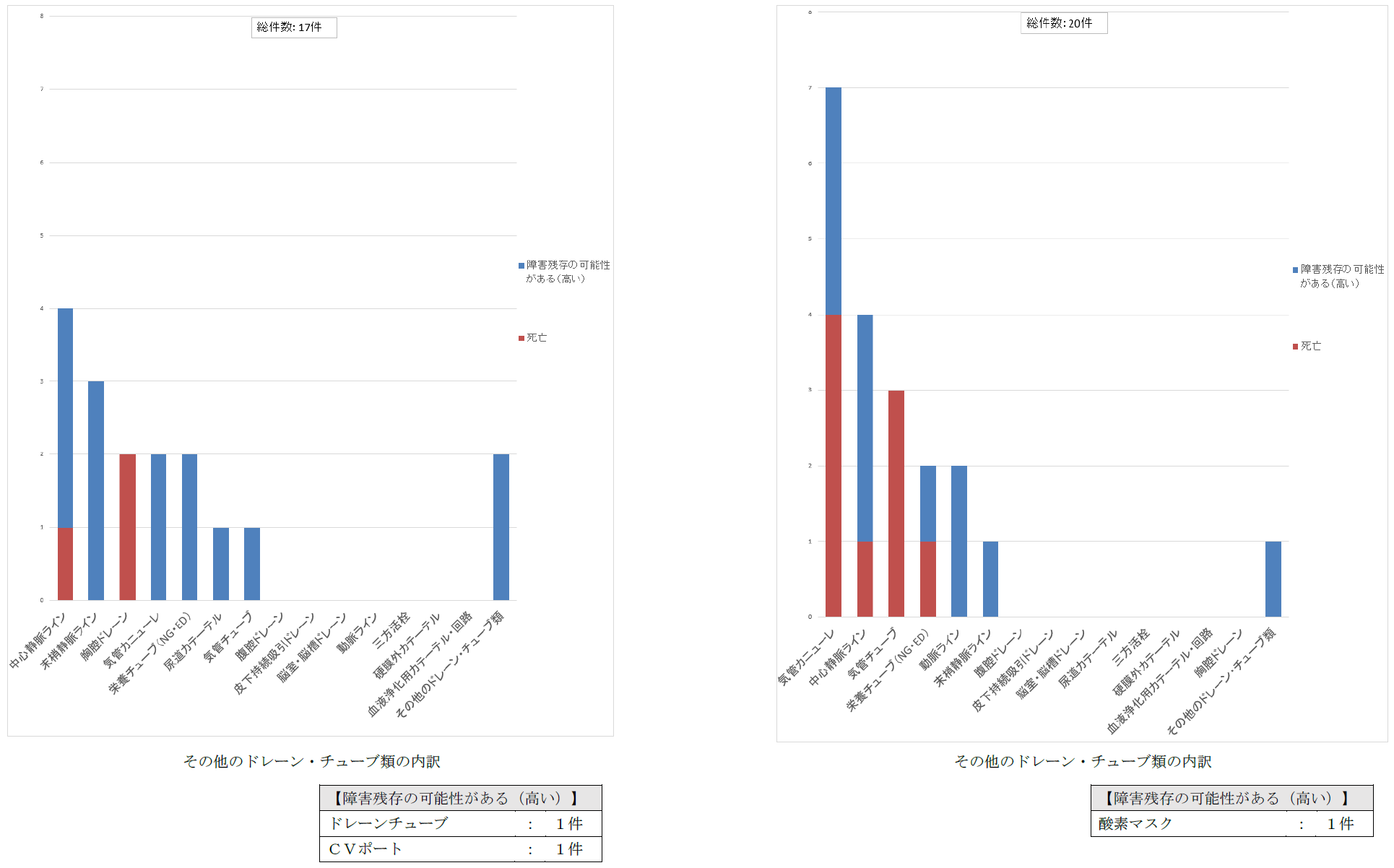
| 種類 | 事故の程度 | 事故の内容 | 別添2 No. |
|---|---|---|---|
| 中心静脈ライン | 死亡 | その他のドレーン・チューブ類の使用に関する内容 | 1 |
| 障害残存の可能性がある(高い) | その他のドレーン・チューブ類の管理に関する内容 その他のドレーン・チューブ類の使用に関する内容 |
2,3 | |
| 動脈ライン | 障害残存の可能性がある(高い) | 使用中の点検・管理ミス | 4 |
| 気管チューブ | 死亡 | その他のドレーン・チューブ類の使用に関する内容 | 5 |
| 気管カニューレ | 死亡 | その他のドレーン・チューブ類の使用に関する内容 | 6,7,8 |
| 障害残存の可能性がある(高い) | 閉塞 その他のドレーン・チューブ類の使用に関する内容 |
9,10 | |
| 栄養チューブ(NG・ED) | 死亡 | その他のドレーン・チューブ類の使用に関する内容 | 11 |
| 障害残存の可能性がある(高い) | その他のドレーン・チューブ類の使用に関する内容 | 12 |
(注)事故の程度が「死亡」又は「障害残存の可能性がある(高い)」事例のみ
図3 ドレーン・チューブ以外の医療機器における事故の内容の内訳
|
集計対象期間:2022年7月1日から12月31日 |
集計対象期間:2023年1月1日から6月30日 |
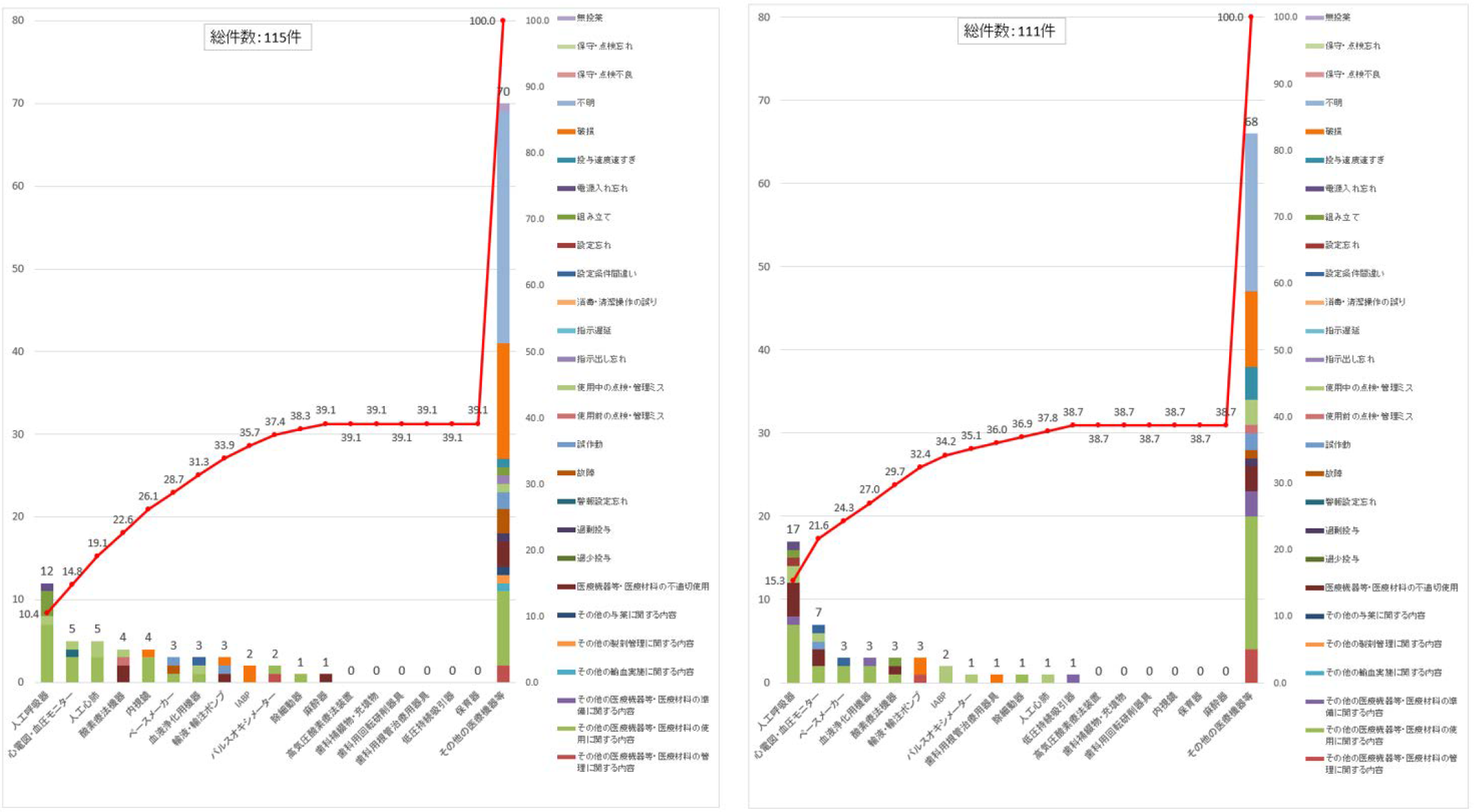
図4 ドレーン・チューブ以外の医療機器における事故の程度の内訳
|
集計対象期間:2022年7月1日から12月31日 |
集計対象期間:2023年1月1日から6月30日 |
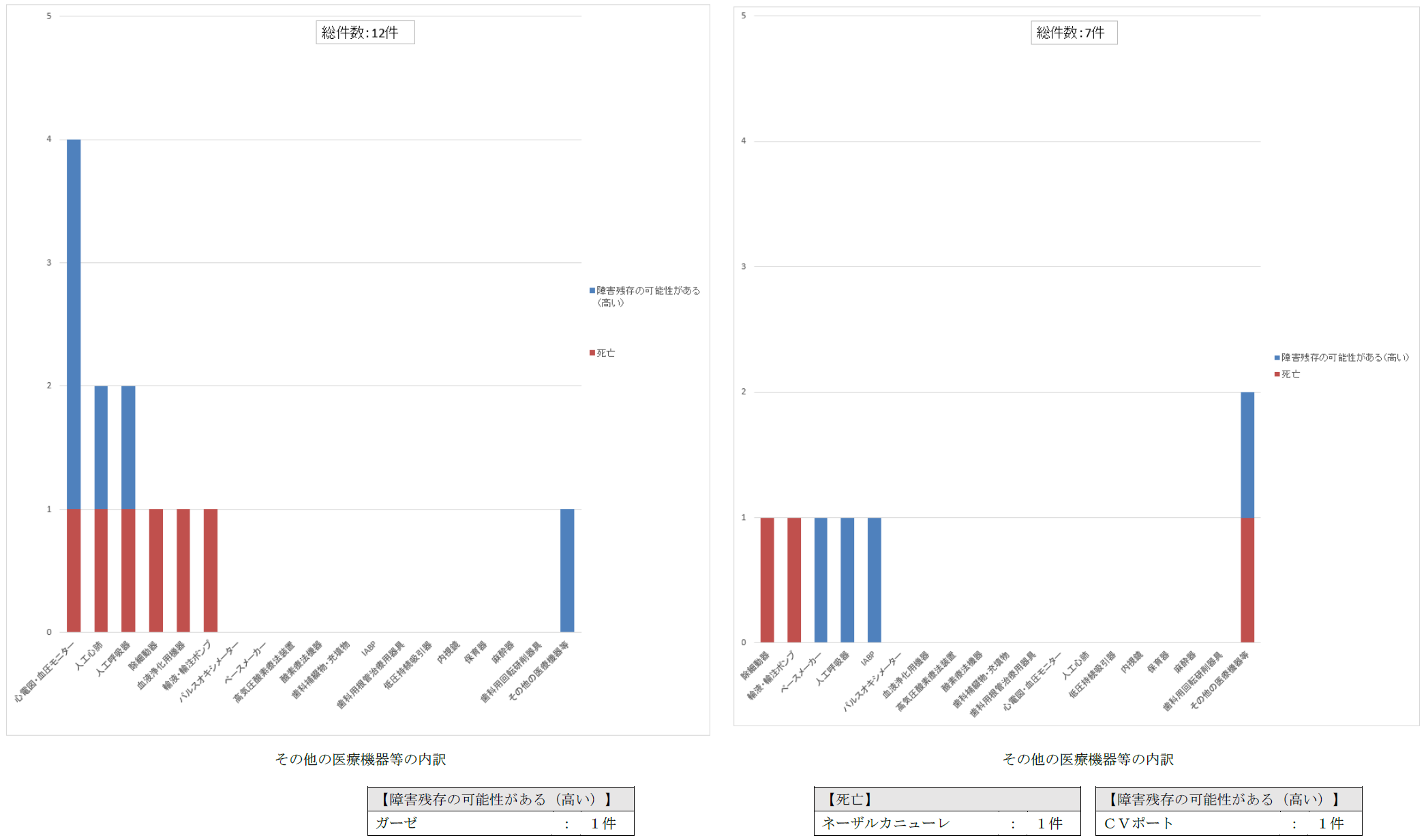
| 種類 | 事故の程度 | 事故の内容 | 別添2 No. |
|---|---|---|---|
| 人工呼吸器 | 障害残存の可能性がある(高い) | その他の医療機器等・医療材料の使用に関する内容 | 13 |
| 輸液・輸注ポンプ | 死亡 | その他の医療機器等・医療材料の管理に関する内容 | 14 |
(注)事故の程度が「死亡」又は「障害残存の可能性がある(高い)」事例のみ
|
参考1 過去に報告されたドレーン・チューブの累積件数 |
参考2 過去に報告されたドレーン・チューブ以外の医療機器の累積件数 |
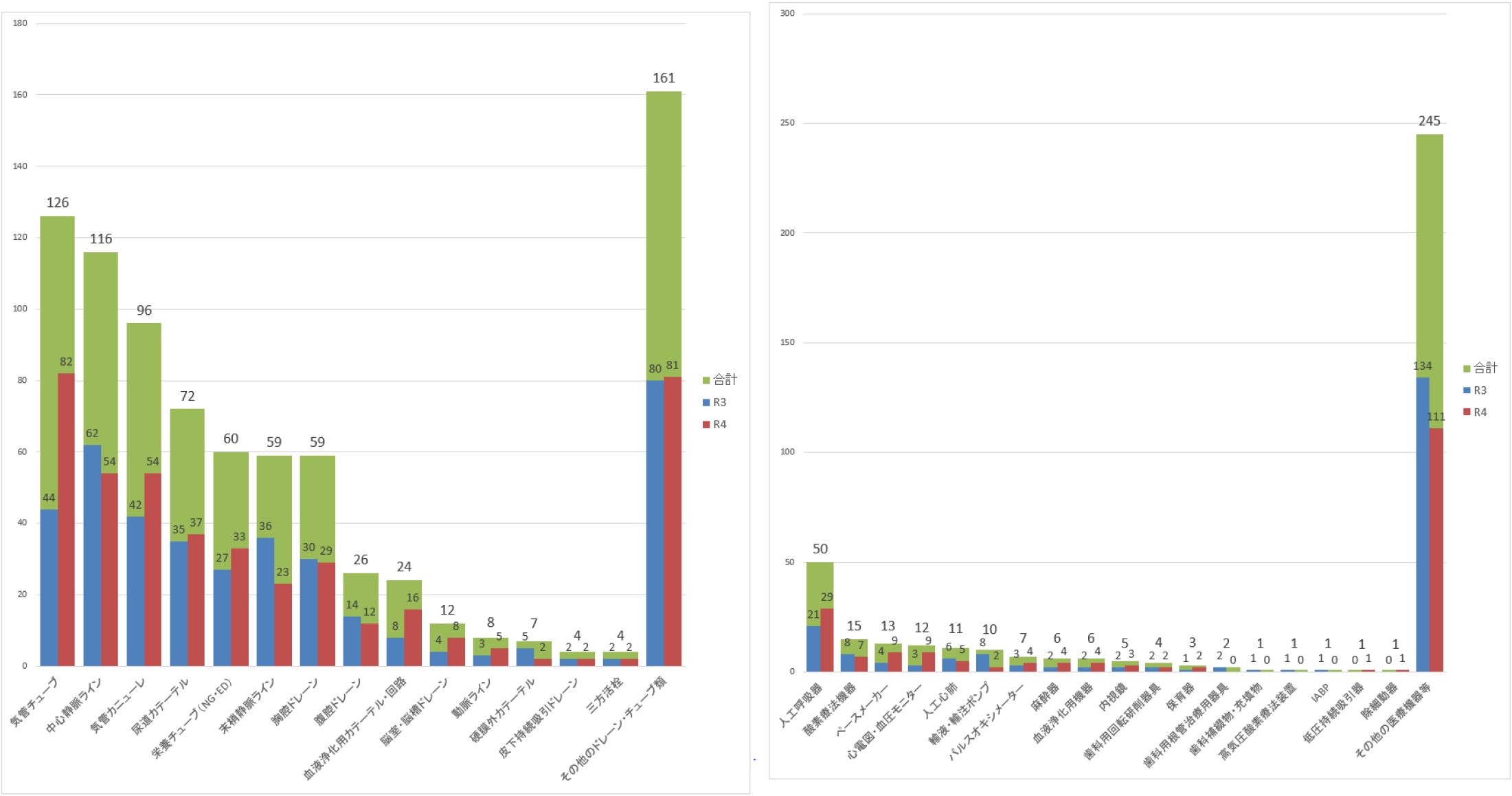
- 同様事例数について
調査対象の各事例において、これまでに同様の事例が集積され、PMDA医療安全情報を作成・配信し、注意喚起を実施している事例と同様の事例数をまとめた結果を表3と表4に示す。
| 分類 | 調査件数 | 同様事例数の内訳 | 事例件数 |
|---|---|---|---|
| 中心静脈ライン | 23 |
|
3 |
| 末梢静脈ライン | 7 | 0 | |
| 動脈ライン | 4 | 0 | |
| 気管チューブ | 49 |
|
4 |
| 気管カニューレ | 40 |
|
12 |
| 栄養チューブ(NG・ED) | 11 |
|
4 |
| 尿道カテーテル | 22 |
|
9 |
| 胸腔ドレーン | 19 |
|
6 |
| 腹腔ドレーン | 10 | 0 | |
| 脳室・脳槽ドレーン | 2 | 0 | |
| 皮下持続吸引ドレーン | 1 | 0 | |
| 硬膜外カテーテル | 4 |
|
1 |
| 血液浄化用カテーテル・回路 | 5 | 0 | |
| その他のドレーン・チューブ類 | 45 |
|
4 |
| 合計 | 242 | 43 |
| 分類 | 調査件数 | 同様事例数の内訳 | 事例件数 |
|---|---|---|---|
| 人工呼吸器 | 17 |
|
5 |
| 酸素療法機器 | 3 | 0 | |
| 人工心肺 | 1 |
|
1 |
| 除細動器 | 1 | 0 | |
| IABP | 2 | 0 | |
| ペースメーカー | 3 | 0 | |
| 輸液・輸注ポンプ | 3 | 0 | |
| 血液浄化用機器 | 3 | 0 | |
| 低圧持続吸引器 | 1 | 0 | |
| 心電図・血圧モニター | 7 |
|
3 |
| パルスオキシメーター | 1 | 0 | |
| 歯科用根管治療用器具 | 1 | 0 | |
| その他の医療機器等 | 68 |
|
8 |
| 合計 | 111 | 17 |
- 安全使用対策の必要性
医療機器の製造販売業者等による安全使用対策の必要性の有無について、調査対象の全353事例の調査結果を表5に示す。
| 類型 | 調査結果 | 事例数 | 割合 |
|---|---|---|---|
| I | 製造販売業者等により、速やかに新たな対策をとる必要がある事例 | 0 | 0.00% |
| II | 製造販売業者等により、既に対策がとられている事例、または既に対策が検討されている事例 | 6 | 1.70% |
| III | 上記以外の事例(事例の集積が必要な事例、ヒューマンエラーによる事例など) | 347 | 98.30% |
| 計 | 353 | 100% |
4. 調査結果の内訳
- 製造販売業者等により、既に対策がとられている事例、または既に対策が検討されている事例(別添1[203.33KB])
- 透析装置のメーカーメンテナンス時のホース屈曲の事例(1番)
- 皮下植込み型ポートのロックリング遺残の事例(2番)
- 手術用ロボットの物理的干渉による意図しない反転移動の事例(3番)
- 皮下植込み型ポートのカテーテル断裂の事例(4から6番)
- ヒューマンエラーによる事例(別添2[915.19KB])
- 事例の集積が必要な事例(別添3[520.96KB])
以上
