要指導・一般用医薬品の相談について
1.1.相談区分及び概要
1. スイッチOTC等開発戦略相談
スイッチOTCや他のOTC(新添加物を含む。)について、(1)OTCとしての開発の妥当性(意義、必要性、効能・効果、用法・用量、投与対象集団に対する有効性、安全性なども含む。)、 (2)生物学的同等性に関する試験計画等の妥当性、(3)新添加物としての妥当性、(4)適正使用に関する資材及び製造販売後調査計画等、新たなOTCの開発戦略について、専門委員の意見も踏まえた上で指導及び助言を行うもの。
対面助言記録等の一部として、相談者が厚生労働省にて開催される「医療用から要指導・一般用への転用に関する評価検討会議」(以下「評価検討会議」という。)へ提出することを目的とした資料を機構が作成し、相談者に伝達する。
当該相談終了後、相談者が希望する場合は、評価検討会議において、機構が相談結果に基づく説明及び質疑応答を行う。
2. スイッチOTC等開発戦略追加相談
スイッチOTC等開発戦略相談を行った上で、申請までに行う2回目以降の相談。
3. スイッチOTC等開発前相談
スイッチOTCや他のOTC(新添加物を含む。)に関し、これまでに得られている安全性情報、有効性情報、海外における承認状況及び類似薬等の情報(申請予定添付資料(概要)も含む。)等に基づき、申請に至るまでに必要な試験、開発計画策定等について、指導及び助言を行うもの。
4. OTC生物学的同等性相談
OTCに関し、既存の生物学的同等性ガイドラインの適用となるものを対象に、試験計画又は試験結果の評価方針の妥当性等に関し資料の十分性等について指導・助言を行うもの。
5. スイッチOTC等製造販売後安全管理相談
スイッチOTCや他のOTCに関し、適正使用の観点から添付文書や情報提供資材の妥当性及び製造販売後調査計画の妥当性等について指導・助言を行うもの。
6. OTC治験実施計画書要点確認相談
OTCに係る治験実施計画書の要点のみについて確認し、指導及び助言を行うもの。データの評価を行うものは該当しない。
7. スイッチOTC等開発妥当性相談
スイッチOTCや他のOTC(新添加物を含む。)に関し、(1)OTCとしての開発の妥当性(意義、必要性、効能・効果、用法・用量、投与対象集団に対する有効性、安全性なども含む。)、(2)新配合剤の配合意義の考え方の妥当性、(3)新添加物としての妥当性等、新たなOTCの開発初期段階における開発の妥当性について、指導及び助言を行うもの。データの評価を行うものは該当しない。
8. 新一般用医薬品開発妥当性相談
(1)OTCとしての効能など、構想段階での開発の妥当性、(2)新配合剤の配合意義の考え方の妥当性、(3)新添加物としての妥当性等、新たなOTCの開発初期段階における開発の妥当性について、指導及び助言を行うもの。データの評価を行うものは該当しない。
9. OTC品質相談
予定する別紙規格、規格及び試験方法に関し、同成分の承認前例と比較する等により、規格を追加する必要性及び規格値の妥当性について、指導及び助言を行うもの。新有効成分又は新添加物は該当しない。
詳細は、実施要綱等通知の別添7[346KB]をご覧ください。
1.2.手数料表
| 相談区分 | 手数料額 |
|---|---|
|
2,500,000円 |
|
1,000,000円 |
|
1,800,000円 |
|
1,000,000円 |
|
700,000円 |
|
700,000円 |
|
600,000円 |
|
300,000円 |
|
300,000円 |
対面助言実施日
当該相談の実施日は、原則として以下のとおりです。その日が祝日にあたる場合は、休みとし、振替は行いません。また、実施日を変更する場合には、事前面談等で事前にお知らせします。
| 区分 | 実施日及び時間帯(枠数) |
|---|---|
|
毎月第4火曜日 午後2時から午後4時まで(1枠) |
|
毎月第2火曜日 午後2時から午後3時まで(1枠) |
|
毎月第1及び第3火曜日(2枠/日)
|
|
毎月第2及び第4火曜日 書面開催(2枠/日) |
注:2026年3月実施分までの新一般用医薬品開発妥当性相談の日程についてはこちら[229KB]をご覧ください。
2027年3月実施分までの新一般用医薬品開発妥当性相談の日程についてはこちら[98.6KB]をご覧ください。
相談の流れ(概要)
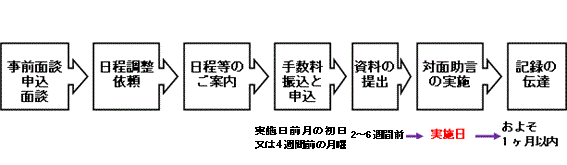
注意事項
申込書等に記載される内容、特にご担当者の連絡先(電話番号、ファクシミリ番号、電子メールアドレス)に間違いがないことをご確認の上、各種書類を提出くださいますようお願いいたします。
3.1.事前面談(必須)
対面助言を円滑に進めるため、事前に相談項目の整理等を行うものです。
本事前面談にて、事前の打ち合わせを行ってください。
事前面談の申込手順等の詳細は、事前面談のWebページをご確認ください。
なお、スイッチOTC等開発戦略相談の実施を希望する場合は、事前面談にて、相談事項、相談資料の内容、専門協議の開催に係る専門委員の利益相反に関する資料(相談資料作成関与委員リスト並びに競合品目リスト及びその関与委員リスト)及びそれらの提出時期等について、機構の担当者と事前の打合せを必ず行ってください。スイッチOTC等開発戦略相談のための事前面談の実施時間は最大で1時間とします。事前面談申込後、可能な範囲で相談資料(案)を提出してください。提出方法及び提出先は、3.5. 資料の提出に従ってください。スイッチOTC等開発戦略相談の手続きを円滑に進めるため、相談資料提出時期の概ね1か月前から3か月前までに事前面談を実施してください。
3.2.日程調整依頼
「医薬品対面助言申込書(要指導・一般用医薬品の相談)」の表題部分を「医薬品対面助言日程調整依頼書(要指導・一般用医薬品の相談)」と書き換え、必要事項を記入し、電子メールにより審査マネジメント部審査マネジメント課に提出してください。
申込先及び問合せ先はこちら
受付時期
- 月曜日から金曜日(国民の祝日等の休日を除く)、午前9時30分から午後5時(厳守)
様式ダウンロード等
様式第5号:医薬品対面助言申込書(要指導・一般用医薬品の相談)
(注) Web会議の実施を希望の場合は、「Web会議による対面助言等の実施に関する基本確認事項」をあわせてご提出ください
- 様式第57号:Web会議による対面助言等の実施に関する基本確認事項
詳細は、「対面助言等におけるWeb会議システム利用要綱」(別添23-2[100KB])をご確認ください。
(注) 相談申込者の押印は不要です。
メール提出時のお願い
- (注)日程調整依頼書は、テキスト認識可能なファイル(PDF等)で提出してください。
- (注)電子メールの件名を次のように記載してください。:日程調整依頼書_会社名、薬剤名等
例)日程調整依頼書_○○製薬、PMD2020A
3.3.日程等のご案内
相談実施日時、場所等が確定した後に、審査マネジメント部より相談者の連絡先あてにファクシミリにてお知らせします。
(注) OTC品質相談は書面開催
3.4.手数料振込と申込
手数料を振り込んだ上で、「医薬品対面助言申込書(要指導・一般用医薬品の相談)」に振込金受取書等の写しを添付の上、電子メールにより審査マネジメント部審査マネジメント課にお申込みください。申込み日時は、「対面助言実施のご案内」により連絡しますが、原則として下記の日時です。
申込み先はこちら
各種手数料についてはこちら
| 区分 | 申込みの受付日及び時間 |
|---|---|
|
原則として相談実施月の前月の第一勤務日 午前10時から正午 |
|
原則として相談希望日の8週間前の月曜日 午前10時から正午 |
|
原則として相談希望日の4週間前の月曜日 午前10時から正午 |
様式ダウンロード等
様式第5号:医薬品対面助言申込書(要指導・一般用医薬品の相談)
- (注)申込書は、テキスト認識可能なファイル(PDF等)で提出してください。
- (注)申込書提出時には電子メールの件名を次のように記載してください。:申込書_受付番号○○(会社名)
3.5.資料の提出
(1)資料の提出方法及び提出先
対面助言の資料については、以下のいずれかの方法により、一般薬等審査部へ提出してください。
- 電子メール(otc_soudan[at]pmda.go.jp)([at]を半角のアットマークに置き換えてください。)
(提出資料の容量が大きい場合には、電子媒体(CD又はDVD)(1部)の郵送)による提出 - 申請電子データシステム(ゲートウェイシステム)を利用したオンライン提出
(2)資料の提出日は、日程等のご案内時に連絡しますが、原則として以下のとおりとします。
- スイッチOTC等開発戦略相談
対面助言実施予定日の原則として6週間前(午後3時まで) - スイッチOTC等開発戦略追加相談
対面助言実施予定日の原則として6週間前(午後3時まで) - スイッチOTC等開発前相談
対面助言実施予定日の原則として6週間前(午後3時まで) - OTC生物学的同等性相談
対面助言実施予定日の原則として5週間前(午後3時まで) - スイッチOTC等製造販売後安全管理相談
対面助言実施予定日の原則として4週間前(午後3時まで) - OTC治験実施計画書要点確認相談
対面助言実施予定日の原則として5週間前(午後3時まで) - スイッチOTC等開発妥当性相談
対面助言実施予定日の原則として4週間前(午後3時まで) - 新一般用医薬品開発妥当性相談
対面助言実施予定日の原則として2週間前(午後3時まで) - OTC品質相談
対面助言実施予定日の原則として3週間前(午後3時まで)
相談資料の提出に際しては以下の留意事項を必ず事前に確認してください。
資料編纂にあたって、以下のお願いを参考にしてください。
また、資料に含める内容は実施要綱7.相談資料に盛り込む内容を参照してください。
搬入される対面助言の資料について[293KB]
対面助言資料のゲートウェイ提出の方法・留意事項[473KB]
なお、相談者側から相談事項の概略についてプレゼンテーションがある場合のプレゼンテーション用資料は、できれば対面助言実施日の1週間前に、遅くとも2勤務日前までに相談担当者に提出してください。
3.6.対面助言の実施
対面助言実施日の前日までに、出席者人数、相談者側専門家又は外国人の出席の有無(通訳出席の有無含む)について、機構の担当者までご連絡ください。
相談者側出席者については、別途連絡がなければ1相談につき、10名以内としてください。
(注) OTC品質相談は書面開催
対面助言のためにお越しになられる皆様へ[9KB]
3.7.記録の伝達
対面助言が終了した後には、相談者に内容を確認の上、機構においてポイントを簡潔に整理した要旨を作成し、相談者に伝達します。
なお、スイッチOTC等開発戦略相談については、相談者が「医療用から要指導・一般用への転用に関する評価検討会議」へ提出することを目的とした資料を機構において作成し、相談者に伝達します。
実施要綱・手数料等関連通知
要指導・一般用医薬品の相談についてのお申込み先及びお問合せ先
独立行政法人 医薬品医療機器総合機構 審査マネジメント部 審査マネジメント課
〒100-0013 東京都千代田区霞が関3-3-2 新霞ヶ関ビル
- 電話(ダイヤルイン) : 03-3506-9556
- ファクシミリ : 03-3506-9443
- 電子メール:shinyaku-uketsuke[at]pmda.go.jp([at]を半角のアットマークに置き換えてください。添付ファイルは10MBまでとしてください。1回のメールで送付できない場合は、受付後に担当者に直接送付してください。)
お問合せに関しては、午前9時30分から午後5時まで(土曜日、日曜日及び国民の祝日を除く)となっております。
