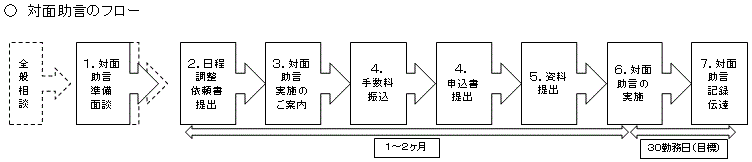
医療機器の対面助言の流れ
1.1.対面助言準備面談(任意)
対面助言に向けて、相談内容を明確化するために、事前打ち合わせするものです。
- 有料、30分
- 面談終了後にPMDAから準備面談終了証を発行します。
- 手順や日程等は、準備面談のページでご確認ください。
注意事項
- 終了証は対面助言の手数料から、準備面談の手数料分を減ずる証明書となり、対面助言の申込時に必要となりますので、紛失しないで下さい。再発行はいたしません。
- 1つの対面助言に対して、準備面談は1回のみ申込みが可能です。
- 終了証の有効期限は1年間です。論点の整理や資料の整備などに時間がかかりそうな場合など、すぐに対面助言に進めることが難しいと判断される場合は、準備面談の前に全般相談をご活用ください。
1.2.日程調整依頼書提出
対面助言を希望する日時を複数記入して、依頼書を提出ください。
提出書類
- 日程調整依頼書
- 医療機器区分用:
- プログラム医療機器区分用:
- プログラム医療機器(検査システム)区分用】:
(注):日程調整依頼書の記載例はこちら[297KB]
- 準備面談終了証の写し(pdfファイル等)
- (Web会議システムの利用を希望する場合)様式第57号:Web会議による対面助言等の実施に関する基本確認事項
Web会議システムの利用を希望する場合の手続きについてはこちらをご覧ください[266KB]
提出方法
電子メールでご提出ください。
電子メールアドレス: kikitaishin-uketsuke[at]pmda.go.jp(審査マネジメント課)
(注):送信の際は[at]を半角のアットマークに置き換えてください。
(注):添付ファイルは10MBまでとしてください。
(注):申込み後、10業務日を経過しても連絡がないときは、電子メール等不着の場合があるため、電話(03-3506-9556)にてご確認をお願いします。
電子メールの件名
医療機器対面助言日程調整依頼書_被験物の名称_企業名
(記載例:医療機器対面助言日程調整依頼書_△△カテーテル_〇〇株式会社)
注意事項
- 日程調整依頼時に、相談資料のメール添付はしないでください。
- 電子メールでの提出が困難な場合、審査マネジメント部審査マネジメント課にご連絡ください。
1.3.対面助言実施のご案内
日程調整した結果について、PMDAから「対面助言のご案内」を送信いたします。1.4.手数料振込、申込書提出
対面助言実施のご案内送付翌日から15勤務日以内又は資料搬入日のいずれか早い日までに振込みの上、審査マネジメント部審査マネジメント課宛に申込書を提出ください。(具体的な締切日は、「対面助言のご案内」を参照ください。)
提出書類
- 申込書
- 医療機器区分用:
- プログラム医療機器区分用:
- プログラム医療機器(検査システム)区分用:
(注):日程調整依頼書を修正することでも可
(注):申込書提出時の確認事項はこちら[301KB]
- 振込金受取書等の写し
- 評価相談を申込む場合にあっては、プロトコル相談記録の写し等(該当する場合のみ)
提出方法
電子メールでお送りください。
電子メールアドレス:kikitaishin-uketsuke[at]pmda.go.jp(審査マネジメント課)
(注):送信の際は[at]を半角のアットマークに置き換えてください。
電子メールの件名
受付番号_被験物の名称_企業名
(記載例:機PXXXX_△△カテーテル_〇〇株式会社) (注):Xには数字が入ります。
注意事項
- 申請時に、相談資料のメール添付はしないでください。
- 電子メールでの提出が困難な場合、審査マネジメント部審査マネジメント課にご連絡ください。
1.5.対面助言資料提出
郵送・配送又は申請電子データシステム(ゲートウェイシステム)のいずれかにより審査マネジメント部審査マネジメント課へご提出ください。ファイルの容量に関わらず、電子メール・オンラインストレージによる提出は受け付けておりません。提出日 (「対面助言のご案内」に記載します)
- 対面助言実施日の2、3又は5週間前の月曜日15時までに搬入(相談区分によって異なります)。
- 事前見解を希望する場合:5週間前搬入。ただし、医療機器評価相談 使用成績評価の場合、7週間前搬入(なお、医療機器拡大治験開始前相談、医療機器開発前相談、医療機器申請資料確定相談及び医療機器IDATEN届出前相談は事前見解の設定がありません)
- 具体的な日程については、当ページの下部でご確認ください(ゴールデンウイークや年末年始等が含まれる場合には、資料搬入日が早まる場合があります)。
提出方法
- 郵送・配送又は申請電子データシステム(ゲートウェイシステム)
- 準備面談済区分の申込の場合には、準備面談終了証の原本(紙)を郵送・配送又は持参によりご提出ください。もし、ご持参される場合は、審査マネジメント部審査マネジメント課まで事前にご連絡ください。
注意事項
1.6.対面助言の実施
対面助言は、面会形式、Web会議形式、又はその両方を組み合わせて実施します。
- 相談時間:1時間から2時間(相談区分による)
- 出席人数:15名以内 (注:目安ですが、出席者を把握するため、必要十分な人数としてください。Web会議においては人数制限はございませんが、出席者確認に時間を要しますので、必要性を検討の上、出席者を決定してください。)
- 記録作成あり
- 録音データの提供あり
- 同時通訳ブースあり(通訳は相談者側で準備) (注:Web会議で同時通訳システムの利用を希望する場合は、相談担当部署にご相談ください。)
- 相談開始時に20分程度のプレゼンテーション実施(資料はなるべく1週間前までに相談担当部署へ送付)
『事前見解あり』の場合
- 原則、助言日の10営業日前までに事前見解を相談者に提示します。
- 原則、助言日の5営業日前までに、相談者は、事前見解に対する回答をご連絡ください。
- 実施日に対面による助言を実施します。ただし、事前見解により相談者の了解が得られた場合には、対面による助言をとりやめ書面による助言を実施することも可能です。
1.7.相談記録作成
対面助言が終了した後に、相談者に内容を確認の上、PMDAにおいて記録を作成し、相談者に伝達いたします。記録確定のための面談を必要に応じて実施する場合があります。
参考
実施要綱:薬機発第0302070号(別添13)[471KB]手数料:対面助言等の手数料のページへ
相談区分:薬機発第0302070号(別紙6)[320KB])
分野:薬機発第0302070号(別紙9)「3.分野」へ
関西テレビ会議システムをご利用の方:関西テレビ会議システムのページへ
Web会議システムをご利用の方:薬機発第0302070号(別添23-2)[100KB]
注意事項
依頼書、申込書に記載される内容、特にご担当者の連絡先(電話番号、ファクシミリ番号、電子メールアドレス)に、お間違いが無いことをご確認の上、依頼書、申込書を提出下さいますようお願いいたします。
体外診断用医薬品の対面助言の流れ
2.1.対面助言準備面談(任意)
対面助言に向けて、相談内容を明確化するために、事前打ち合わせするものです。
- 有料、30分
- 面談終了後にPMDAから準備面談終了証を発行します。
- 手順や日程等は、準備面談のページでご確認ください。
注意事項
- 終了証は対面助言の手数料から、準備面談の手数料分を減ずる証明書となり、対面助言の申込時に必要となりますので、紛失しないで下さい。再発行はいたしません。
- 1つの対面助言に対して、準備面談は1回のみ申込みが可能です。
- 終了証の有効期限は1年間です。論点の整理や資料の整備などに時間がかかりそうな場合など、すぐに対面助言に進めることが難しいと判断される場合は、準備面談の前に全般相談をご活用ください。
2.2.日程調整依頼書提出
対面助言を希望する日時を複数記入して、依頼書を提出ください。
提出書類
- 医療機器・体外診断用医薬品対面助言日程調整依頼書
(注):日程調整依頼書の記載例はこちら[297KB]
- 準備面談終了証の写し(pdfファイル等)
- (Web会議システムの利用を希望する場合)様式第57号:Web会議による対面助言等の実施に関する基本確認事項
Web会議システムの利用を希望する場合の手続きについてはこちらをご覧ください[266KB]
提出方法
電子メールでご提出ください。
電子メールアドレス: kikitaishin-uketsuke[at]pmda.go.jp(審査マネジメント課)
(注):送信の際は[at]を半角のアットマークに置き換えてください。
(注):添付ファイルは10MBまでとしてください。
(注):申込み後、10業務日を経過しても連絡がないときは、電子メール等不着の場合があるため、電話(03-3506-9556)にてご確認をお願いします。
電子メールの件名
体外診断用医薬品対面助言日程調整依頼書_被験物の名称_企業名
(記載例:体外診断用医薬品対面助言日程調整依頼書_△△検査薬_〇〇株式会社)
注意事項
- 日程調整依頼時に、相談資料のメール添付はしないでください。
- 電子メールでの提出が困難な場合、審査マネジメント部審査マネジメント課にご連絡ください。
2.3.対面助言実施のご案内
日程調整した結果について、PMDAから「対面助言のご案内」を送信いたします。2.4.手数料振込、申込書提出
対面助言実施のご案内送付翌日から15勤務日以内又は資料搬入日のいずれか早い日までに振込みの上、審査マネジメント部審査マネジメント課宛に申込書を提出ください。(具体的な締切日は、「対面助言のご案内」を参照ください。)
提出書類
- 医療機器・体外診断用医薬品対面助言申込書
(注):申込書提出時の確認事項はこちら[301KB]
- 振込金受取書等の写し
- 評価相談を申込む場合にあっては、プロトコル相談記録の写し等(該当する場合のみ)
提出方法
電子メールでお送りください。
電子メールアドレス:kikitaishin-uketsuke[at]pmda.go.jp(審査マネジメント課)
(注):送信の際は[at]を半角のアットマークに置き換えてください。
電子メールの件名
受付番号_被験物の名称_企業名
(記載例:機PXXXX_△△検査薬_〇〇株式会社) (注):Xには数字が入ります。
注意事項
- 申請時に、相談資料のメール添付はしないでください。
- 電子メールでの提出が困難な場合、審査マネジメント部審査マネジメント課にご連絡ください。
2.5.対面助言資料提出
郵送・配送又は申請電子データシステム(ゲートウェイシステム)のいずれかにより審査マネジメント部審査マネジメント課へご提出ください。ファイルの容量に関わらず、電子メール・オンラインストレージによる提出は受け付けておりません。提出日 (「対面助言のご案内」に記載します)
- 対面助言実施日の2又は3週間前の月曜日15時までに搬入(相談区分によって異なります)。
- 事前見解を希望する場合:5週間前搬入。(なお、体外診断用医薬品開発前相談及び体外診断用医薬品IDATEN届出前相談は事前見解の設定がありません)
- 具体的な日程については、当ページの下部でご確認ください(ゴールデンウイークや年末年始等が含まれる場合には、資料搬入日が早まる場合があります)。
提出方法
- 郵送・配送又は申請電子データシステム(ゲートウェイシステム)
- 準備面談済区分の申込の場合には、準備面談終了証の原本(紙)を郵送・配送又は持参によりご提出ください。もし、ご持参される場合は、審査マネジメント部審査マネジメント課まで事前にご連絡ください。
注意事項
2.6.対面助言の実施
対面助言は、面会形式、Web会議形式、又はその両方を組み合わせて実施します。
- 相談時間:1時間から2時間(相談区分による)
- 出席人数:15名以内 (注:目安ですが、出席者を把握するため、必要十分な人数としてください。Web会議においては人数制限はございませんが、出席者確認に時間を要しますので、必要性を検討の上、出席者を決定してください。)
- 記録作成あり
- 録音データの提供あり
- 同時通訳ブースあり(通訳は相談者側で準備) (注:Web会議で同時通訳システムの利用を希望する場合は、相談担当部署にご相談ください。)
- 相談開始時に20分程度のプレゼンテーション実施(資料はなるべく1週間前までに相談担当部署へ送付)
『事前見解あり』の場合
- 原則、助言日の10営業日前までに事前見解を相談者に提示します。
- 原則、助言日の5営業日前までに、相談者は、事前見解に対する回答をご連絡ください。
- 実施日に対面による助言を実施します。ただし、事前見解により相談者の了解が得られた場合には、対面による助言をとりやめ書面による助言を実施することも可能です。
2.7.相談記録作成
対面助言が終了した後に、相談者に内容を確認の上、PMDAにおいて記録を作成し、相談者に伝達いたします。記録確定のための面談を必要に応じて実施する場合があります。
参考
実施要綱:薬機発第0302070号(別添13)[467KB]手数料:対面助言等の手数料のページへ
相談区分:薬機発第0302070号(別紙6)[316KB])
分野:薬機発第0302070号(別紙9)「3.分野」へ
関西テレビ会議システムをご利用の方:関西テレビ会議システムのページへ
Web会議システムをご利用の方:薬機発第0302070号(別添23-2)[100KB]
注意事項
依頼書、申込書に記載される内容、特にご担当者の連絡先(電話番号、ファクシミリ番号、電子メールアドレス)に、お間違いが無いことをご確認の上、依頼書、申込書を提出下さいますようお願いいたします。
資料搬入の日程について
お申込先及びお問合せ先
独立行政法人 医薬品医療機器総合機構 審査マネジメント部 審査マネジメント課
〒100-0013 東京都千代田区霞が関3-3-2 新霞ヶ関ビル
- 電話:03-3506-9556
- ファクシミリ:03-3506-9443
- 電子メール:kikitaishin-uketsuke[at]pmda.go.jp([at]を半角のアットマークに置き換えてください。添付ファイルは10MBまでとしてください。1回のメールで送付できない場合は、受付後に担当者に直接送付してください。)
お問合せに関しては、午前9時30分から午後5時まで(土曜日、日曜日及び国民の祝日を除く)となっております。

 [11KB]
[11KB]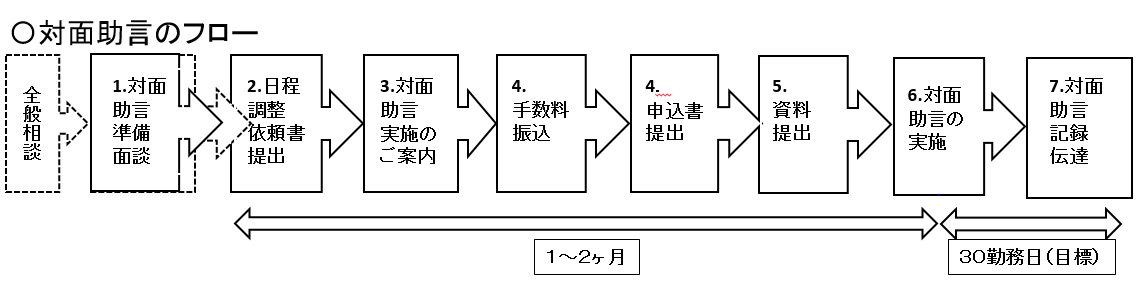 [46KB]
[46KB]